来源:光华所检索分析咨询部 发布时间:2023-12-28 10:02 点击量:4059
生物大分子专利是生物化学领域非常重要的一类专利,是生物大分子药物的研究基础,因此生物大分子相关专利的授权和侵权得到药企的关注。涉及生物序列的技术方案的实施,都有潜在的专利侵权风险。值得关注的是,企业自身拥有大分子序列的专利,不代表这个序列相关的产品不会在当地发生侵犯别人专利的风险。大分子药物序列的可专利性标准和侵权判定标准是完全不同的两个概念。
生物大分子专利一般首先会通过氨基酸或者核苷酸序列进行保护,权利要求常写为特定的序列或具有一定的开放式序列(同源性等),撰写方式不同会导致FTO关注的重点不同。
本文尝试通过生物序列的不同限定方式探讨在授权和侵权判定过程中应当考量的因素,以帮助在专利申请之初更谨慎选择生物序列专利的限定方式,帮助获得授权和更好进行维权。
受限于篇幅,授权和侵权过程将分为两文发布,本文将着重探讨生物序列专利的限定方式对专利授权的影响。后文将继续对不同生物序列限定方式专利的侵权判定方式进行探讨。
一、生物序列的限定方式
根据保护范围的不同,涉及生物序列的专利权利要求的限定方式不同。《专利审查指南》中对涉及基因、载体、重组载体、转化体、多肽或蛋白质、融合细胞和单克隆抗体等遗传工程的发明权利要求的限定方式进行了说明。
其中,基因、多肽或蛋白质和微生物的权利要求限定方式描述如下。
1.1 基因的限定方式
(1)直接限定其碱基序列。
(2)对于结构基因,可限定由所述基因编码的多肽或蛋白质的氨基酸序列。
(3)当该基因的碱基序列或其编码的多肽或蛋白质的氨基酸序列记载在序列表或说明书附图中时,可以采用直接参见序列表或附图的方式进行描述。
例如:
一种DNA分子,其碱基序列如SEQIDNO:1(或附图 1)所示。
(4)对于具有某一特定功能,例如其编码的蛋白质具有酶A活性的基因,可采用术语“取代、缺失或添加”与功能相结合的方式进行限定。
例如:
编码如下蛋白质(a) 或(b) 的基因:
(a)由Met-Tyr-… -Cys-Leu所示的氨基酸序列组成的蛋白质,
(b)在(a) 限定的氨基酸序列中经过取代、缺失或添加一个或几个氨基酸且具有酶A活性的由(a) 衍生的蛋白质。
(5)对于具有某一特定功能,例如其编码的蛋白质具有酶A活性的基因,可采用在严格条件下“杂交”,并与功能相结合的方式进行限定。
例如:
如下(a) 或(b) 的基因:
(a)其核苷酸序列为ATGTATCGG… TGCCT所示的DNA分子;
(b)在严格条件下与(a) 限定的DNA序列杂交且编码具有酶A活性的蛋白质的DNA分子。
(6)当无法使用前述五种方式进行描述时,通过限定所述基因的功能、理化特性、起源或来源、产生所述基因的方法等描述基因才可能是允许的。
1.2多肽或蛋白质的限定方式
(1)限定氨基酸序列或编码所述氨基酸序列的结构基因的碱基序列。
(2)当其氨基酸序列记载在序列表或说明书附图中时,可以采用直接参见序列表或附图的方式进行描述。
例如:
一种蛋白质,其氨基酸序列如SEQIDNO:2(或附图 2)所示。
(3)对于具有某一特定功能,例如具有酶A活性的蛋白质,可采用术语“取代、缺失或添加”与功能相结合的方式进行限定,具体方式如下:
例如:
如下(a) 或(b) 的蛋白质:
(a)由Met-Tyr-… -Cys-Leu所示的氨基酸序列组成的蛋白质;
(b)在(a)中的氨基酸序列经过取代、缺失或添加一个或几个氨基酸且具有酶A活性的由(a)衍生的蛋白质。
(4)当无法使用前述三种方式进行描述时,采用所述多肽或蛋白质的功能、理化特性、起源或来源、产生所述多肽或蛋白质的方法等进行描述才可能是允许的。
1.3 微生物的限定方式
(1)权利要求中所涉及的微生物应按微生物学分类命名法进行表述,有确定的中文名称的,应当用中文名称表述,并在第一次出现时用括号注明该微生物的拉丁文学名。如果微生物已在国家知识产权局认可的保藏单位保藏,还应当以该微生物的保藏单位的简称和保藏编号表述该微生物。
(2)如果说明书中没有提及某微生物的具体突变株,或者虽提及具体突变株,但是没有提供相应的具体实施方式,而权利要求中却要求保护这样的突变株,则不允许。
从限定方式可以看出,对于序列的限定方法有封闭式和开放式的限定方法,封闭式的限定方法即直接限定到具体的序列,而开放式限定方法会通过过规则对基础序列进行一定范围的变化,例如通过上述的“取代、缺失或添加一个或几个氨基酸”的限定方式,或者通过“序列同源性”进行限定。
对于如何限定涉及生物序列的相关权利要求,平衡专利权人与社会公众利益,一直是专利实践中争议较大的内容。专利权人认为,将生物序列限定为封闭式的、特定具体序列,由于保护范围过小,很容易被他人绕开,不利于专利权的保护。而审查员则认为,由于生物领域较低的可预见性,将生物序列撰写为开放式限定的序列无法得到说明书的支持。开放式生物序列的限定包括了大量序列不同的生物序列,同时由于生物序列的构效关系非常复杂、可预见性低。笔者个人认为在未经试验逐一验证的情况下,开放式限定方式存在难以获得说明书的支持,进而难以获得授权的问题。
生物序列权利要求的开放性限定如何得到说明书支持是本文探讨的重要内容之一。本文将通过审查结果的检索调查对这个问题进行探讨。
二、“同源性”限定方式的支持问题
笔者采用商用数据库对“同源性”限定方式的生物序列相关专利进行了检索和分析以支持本文的结论。截止2023年12月8日的数据如下所示:
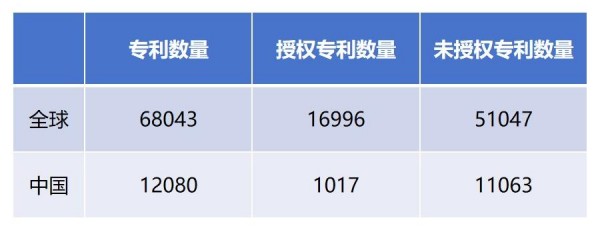
针对专利授权阶段同源性限定的支持问题,不同专利局对其采用“同源性”方式限定权利要求的审查标准严格程度不同,最终给予了不同的授权范围。
笔者下面选取了以下两组简单同族的授权专利作为代表进行分析。对于中国申请号CN200780003441.5,名称为“同型乳酸的嗜热芽抱杆菌的遗传修饰”的专利申请,申请人将该发明分别向中、美、欧、日四局提出专利申请。对于中国申请号CN200580018846.7,名称为“新的螨变应原”的专利申请,申请人将该发明分别向中、韩、欧、日四局提出专利申请。可以看到,不同专利局对其采用“同源性”方式限定的权利要求最终给予了不同的授权范围。横向比较来看,美国对于该类权利要求的支持性审查最为宽松,欧洲审查标准严格程度次之。而中国对生物序列类权利要求的支持性审查标准严格程度略高于日本、韩国。中国对同源性限定授权的审查标准严于其他专利局。
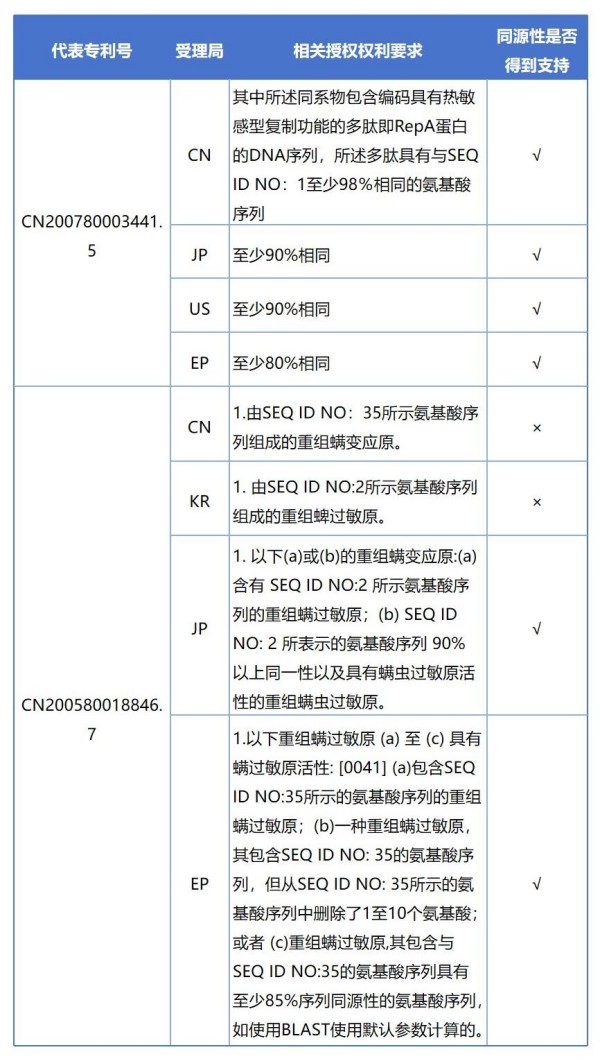
针对同源性的支持问题,最高人民法院也在无效阶段的司法实践中明确了使用同源性加上来源和功能限定方式的生物序列权利要求得到说明书支持的判断规则和生物序列发明专利的授权标准。最高人民法院于2016年12月30日做出(2016)最高法行再85号判决(以下简称第85号判决)给出了判定,对江苏博立生物制品有限公司(以下简称博立生物)诉国家知识产权局专利复审委员会(以下简称复审委),涉及诺维信公司的“热稳定的葡糖淀粉酶”专利有效性做出再审判决,维持了复审委做出的17956号无效宣告请求审查决定。该案作为2016年中国法院10大知识产权案件之一,明确了采用“如SEQ ID NO:XX所示序列(即封闭式撰写方式)”+“功能性限定”+“具体来源限定(例如限定至“种”)”+“序列同源性限定”的撰写方式是可以得到说明书支持的。其相关权利要求如下。

第85号判决给出的理由摘录如下:“权利要求13和14包含有权利要求12中的功能性特征-编码表现出葡糖淀粉酶活性的酶,在序列(a)或(b)无限延伸之后已不具备该功能的DNA序列并未包含于权利要求13和14的保护范围之内。而且,权利要求13和14还分别限定了所述DNA序列来源于T.emersonii菌种和特定菌株T.emersonii CBS793.97,而能够从前述菌种甚至特定菌株中得到的包含序列(a)或序列(b)的DNA序列也是确定的和极少数的。因此,权利要求13和14中引用权利要求12(a)(b)的技术方案能够得到说明书的支持”。“而对于权利要求10和11,如果其如权利要求6所示,没有进一步限定所述酶的菌种或者菌株来源以及酶的功能,第85号判决认为其保护范围将扩展至任意与SEQ ID NO:7具有99%以上同源性的酶序列,本领域技术人员无法得知上述众多的酶序列是否都具备葡糖淀粉酶活性,因此,权利要求6得不到说明书的支持。然而,在权利要求10和11进一步限定所述葡糖淀粉酶来源于前述菌种甚至特定菌株的情况下,其保护范围只是极其有限的序列,甚至更可能仅仅是SEQ ID NO:7本身,因此,采用同源性加上功能和来源限定的权利要求10、11可以得到说明书的支持”。
最高人民法院在本案中明确了使用同源性加上来源和功能限定方式的生物序列权利要求得到说明书支持的判断规则和生物序列发明专利的授权标准,对蛋白质、基因相关专利申请的撰写和审查具有指导意义,也有利于促进生物技术产业的创新和发展。
综合授权阶段和无效阶段对于同源性限定的审查尺度,笔者总结了同源性限定的权利要求要想在中国获得授权并维持稳定的权利,一般需要至少满足三点条件:
① 需要将同源性数值限定在较高的百分比。首先,氨基酸序列的过大变化可能导致多肽的活性或功能丧失或改变;其次,如果改变的氨基酸残基是任意数目和任意类型的,大量氨基酸的变化使得空间结构和结构域很可能会随之发生改变,甚至可能会使目的多肽结构域不能暴露在分子空间结构的表面,从而使原序列丧失功能;再次,变化的氨基酸残基可能会形成其他相互作用如盐键、氢键、二硫键等等从而导致多肽结构域改变或被破坏,甚至功能丧失。因此,如果同源性差异过大可能会导致功能和活性的丧失。
② 需要进行功能性限定,即使用功能的限定。通过功能性限定使得权利要求限定的一系列可变序列能够实现权利要求技术方案解决的技术问题,并且通过功能性限定可以将同源性扩展出的一系列可变序列限定在及其有限的选择范围内,避免出现不符合发明目的的保护范围。
③ 其他能够限定同源性序列变化不会使其丧失原始功能的特征限定,例如序列来源限定,例如保守区域的限定等。作为蛋白质一级结构的氨基酸序列是其空间结构的基础,而蛋白质的空间结构又是其功能的基础,同源性较高的蛋白质是否具有相似的空间结构和相似的功能,主要取决于那些在维系其空间结构以及功能、活性中起关键作用的氨基酸残基的差异,以及这些差异是否足以改变其空间构象和相应的生物学功能及活性,如果蛋白质氨基酸序列中的一些甚至一个起关键作用的氨基酸改变,就会导致蛋白质空间结构与生物学活性或功能的巨大变化,所以,所属技术领域人员无法确定该序列加上同源性限定的该范围包含的所有多肽(例如不同来源的或者功能核心区的氨基酸变化)都能实现本发明的目的。
第③点限定的缺失实际是大部分同源限定在专利审查过程中被认定为得不到说明书支持的主要原因。加强该部分的限定有助于提高同源序列的效果可预期性。
三、针对抗体“同源性”限定的支持问题
在获得授权的1017件“同源性”限定的中国专利中,有183件专利为抗体专利。
对获得授权的抗体专利进行分析,发现基本是以类似如下例的撰写方式进行同源性限定的。
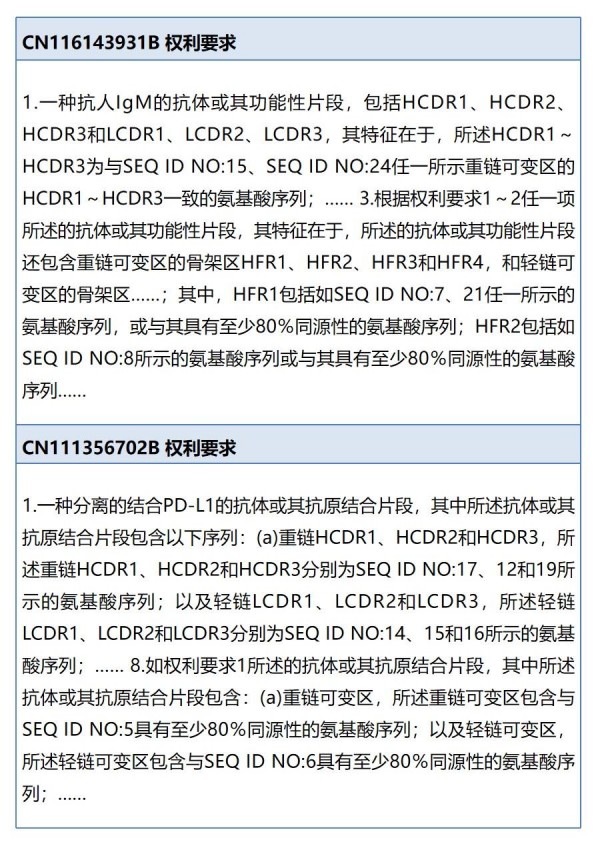
因此,我们可以窥见,现在对于抗体专利采用同源性限定的支持问题的审查标准其实是比较明晰的:在抗体领域,同源性限定在重轻链可变区,并且重轻链可变区的CDR区域作为保守区域是可以得到支持授权的。在此基础上,重轻链可变区的同源性在80%以上都是可以被接受的,只要能够在说明书实施例中对低同源性的序列进行效果的对比验证,甚至低于80%的同源性限定也是可以去尝试的。将CDR区域作为保守区域保证了重轻链可变区的同源性变化在框架区,从而不会丧失原始抗体的活性和功能,也就是做到了本文第二部分总结的第3)点“其他能够限定同源性序列变化不会使其丧失原始功能的特征限定”。
四、“取代、缺失或添加”限定方式的支持问题
笔者采用商用数据库对“取代、缺失或添加”限定方式的生物序列相关专利进行了检索和分析以支持本文的结论。截止2023年12月8日的数据如下所示:
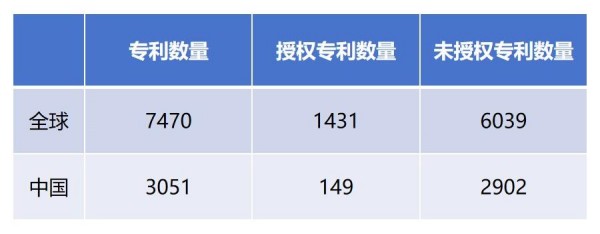
可见,虽然“取代、缺失或添加一个或几个氨基酸”的限定方式是在审查指南中明确可以采用的描述方法,但是,采用这种方式限定的专利相对于“同源性”限定要少的多。
从“取代、缺失或添加一个或几个氨基酸”和“同源性”的表达含义上来看,两者的内涵其实是一样的,都是在基础序列基础上对其进行了开放性限定,“取代、缺失或添加的氨基酸的数量”和“同源性百分比”的数值决定了序列的可变化程度,而这种可变化程度也体现为序列可能的结构和功能的变化程度,两者其实只是表达方式的不同。之所以采用“取代、缺失或添加”限定方式比较少的原因可能是本领域技术人员对于序列相似的表达习惯更多采用同源性进行表达,这也就反映到了专利的表达方式上。
因此,笔者认为“取代、缺失或添加”限定方式同样应该遵循类似于“同源性”限定总结的3点规则才可以得到获得说明书中的支持。
当然,在检索过程中,也发现一些没有遵循上述规则仍然能够获得授权的专利。例如,抗原序列、用途等方法类专利、核苷酸序列在开放式限定上的审查尺度就相对比较宽松,在这些领域的审查尺度相对宽松的原因可能是因为序列的改变对于发明目的的实现影响是相对较小的,例如抗原某些氨基酸的改变对于抗原活性的影响、氨基酸改变对于基本用途的改变、兼并密码子的存在造成的核苷酸的变化,这些变化对于发明目的的实现影响都不是决定性的。例如,CN114409802B为抗原序列专利,其授权权利要求6限定了:由(1)抗原氨基酸序列经取代、缺失或添加一个氨基酸或更多个氨基酸且不改变(1)的抗原性的由(1)衍生的多肽或其类似物,且自身能够形成三聚体。例如用途等方法类专利的同源性限定:CN113528567B为应用类专利,其授权权利要求1限定了:FBA8蛋白或氨基酸序列经取代、缺失或添加一个或几个氨基酸的由FBA8蛋白衍生的蛋白质在调节植物维管束分裂和/或花序轴横截面积中的应用,所述FBA8蛋白的氨基酸序列如SEQ ID NO.1所示。
以上分析是基于大部分生物序列专利授权和确权审查结果的探讨,不排除还有其他例外情况,在专利申请过程中可以借鉴本文的分析结果,并结合专利具体情况进行生物序列限定方式的调整,在获得权利要求支持的情况下争取更大且更稳定的权利保护范围。











